Hoy Consultorsalud pone a su disposición la Guía de Estabilidad de medicamentos biológicos, cuyo trámite se encuentra ya descrito en el plan de trabajo para la reglamentación del Decreto 1782 de 2014, que está en calidad de proyecto normativo, y terminó su fase de recibo de opiniones ante el Minsalud el pasado 9 de junio.
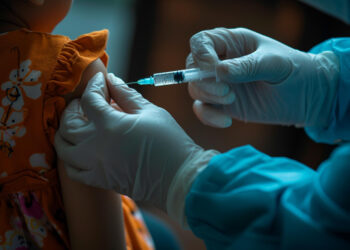
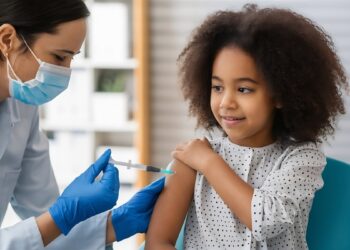
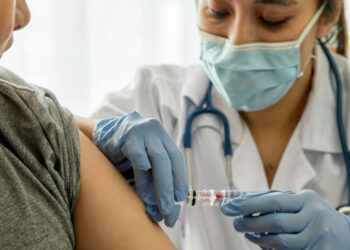
El 18 de septiembre de 2014 se firmó el Decreto 1782 de medicamentos biológicos que regula su registro sanitario, garantizando la seguridad y eficacia de este tipo de medicinas y permitiendo a los pacientes disponer de alternativas terapéuticas de igual calidad y menor precio.
Uno de los aspectos más importantes del decreto 1782 de 2014, tiene relación con las tres rutas de presentación de información: una es la del expediente completo para los medicamentos biológicos nuevos y las otras dos rutas son para los biogenéricos.
La ruta del expediente completo exige un paquete de pruebas pre-clínicas y clínicas que implica extensos y complejos experimentos con animales y humanos sanos y enfermos.
Por su parte, la ruta de la comparabilidad es para medicamentos que no son nuevos, pero que todavía no son suficientemente conocidos, por lo cual se exigen estudios pre-clínicos y clínicos comparativos con el medicamento nuevo. Dada la incertidumbre sobre el comportamiento de la sustancia activa, debe probarse que el mismo funciona en el cuerpo igual que lo hace el medicamento nuevo.
Consultorsalud quiere recordar que al regular la entrada de otros competidores al mercado de medicamentos biotecnológicos, el sistema de salud se ahorrará, en los 8 medicamentos más recobrados, entre $300.000 y $600.000 millones.
Descargue la Guía de Estabilidad de Medicamentos Biológicos